Les organismes de réglementation de Santé Canada ont approuvé aujourd’hui l’utilisation du dispositif de test rapide ID NOW COVID-19 dans ce pays – une mesure qui pourrait entraîner des millions de tests supplémentaires pour les communautés aux prises avec une augmentation subite des cas de coronavirus.
Cette approbation intervient seulement un jour après que le gouvernement fédéral ait annoncé qu’il achèterait quelque 7,9 millions de tests ID NOW à l’entreprise américaine pour les distribuer au Canada.
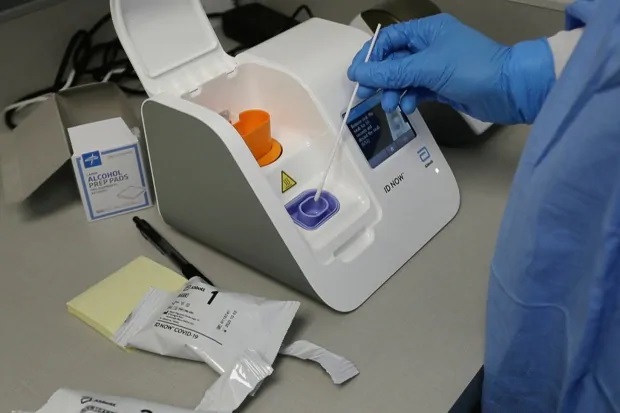
(Carlos Osorio/AP Photo)
Le test rapide développé par le groupe pharmaceutique Abbott détecte à partir d’un prélèvement nasal la présence d’antigènes dans le corps d’une personne qui est infectée par le coronavirus. Puisqu’il ne nécessite pas le recours à un laboratoire pour l’analyse des données, il peut produire des résultats en 13 minutes seulement.
Ces tests peuvent donc être utilisés hors des hôpitaux, directement dans les résidences pour personnes âgées, au sein des écoles et même dans les maisons privées. Ces accès plus larges et rapides sont vus comme un moyen de prévenir la propagation de la COVID-19 alors que les centres de dépistage au Canada font face à des vagues humaines et sont mis à rude épreuve.

L’échantillonneur développé par le groupe pharmaceutique Abbott pour son test d’antigènes du virus.
PHOTO : GETTY IMAGES / SPENCER PLATT
Montée d’une deuxième vague au Canada
Jusqu’à présent, la grande majorité des tests sont effectués dans des cliniques de santé publique, les échantillons étant ensuite envoyés aux laboratoires pour analyse – un processus qui peut prendre plusieurs jours. Ces retards font perdre en ce moment un temps très précieux aux autorités sanitaires qui doivent faire la recherche de contacts des personnes infectées alors que les cas de contagion s’avèrent être de plus en plus nombreux.
D’expliquer la ministre canadienne des Services publics, Anita Anand, « Ces tests rapides permettront de répondre aux demandes urgentes des provinces et territoires de tester les Canadiens et de réduire le temps d’attente des résultats, ce qui est essentiel pour réduire la propagation du virus ».
Mme Anand a déclaré , mardi, cependant qu’elle ne pouvait pas préciser quand ces tests seront déployés dans des provinces comme l’Ontario et le Québec, où les files d’attente de plusieurs heures sont une préoccupation montante.
Le nombre de diagnostics positifs continuait d’augmenter partout au Canada, mardi, avec près de 800 nouveaux cas au Québec et plus de 500 en Ontario.
Au Québec, lundi, le ministère provincial de la Santé et des Services sociaux du Québec s’est vu forcé d’annoncer que seules les personnes présentant des symptômes de la COVID-19 ou celles ayant eu un contact étroit avec une personne atteinte de la maladie seraient désormais prioritaires pour la prise de tests. « L’accès au dépistage pourrait être refusé à une personne qui ne fait pas partie des clientèles priorisées », précisait le ministère dans un communiqué.

Alors que la province continue d’essayer de freiner la propagation de COVID-19, les gens font la queue devant un site de test à Montréal. (Ryan Remiorz/La Presse Canadienne)
Quand le chef d’orchestre est Santé Canada
Anita Anand, la ministre canadienne des Services publics a réitéré, mardi, que l’utilisation des nouveaux tests rapides de la compagnie Abbott était assujettie à l’approbation de Santé Canada. Il fallait, selon elle, attendre le feu vert de ses scientifiques pour savoir si ce produit est suffisamment efficace ou sécuritaire.

(Justin Tang/Canadian Press)
« Comme pour beaucoup de nos accords concernant les équipements, les tests et les vaccins, nous avons conclu un accord d’achat anticipé pour garantir l’accès du Canada à ces tests, sous réserve de l’approbation réglementaire de Santé Canada », a déclaré Madame Anand.
Plusieurs au pays critiquent ce processus de vérification qui leur semble long alors que Food and Drug Administration américaine a approuvé des douzaines de dispositifs de test rapides. Au Canada, un seul de ces produits a été approuvé, la semaine dernière, et ce sur une douzaine de produits en attente d’approbation.
La FDA américaine a délivré une autorisation d’utilisation d’urgence à Abbott pour le test que le Canada a acheté en mars dernier.
Certains chercheurs ont cependant déclaré que le dispositif d’Abbott a conduit à de faux positifs dans un petit nombre de cas. L’approbation d’un dispositif qui ne produirait pas de résultats précis pourrait, en fait, propager la COVID-19. Selon les critères de Santé Canada, un test doit être précis à au moins 80 % pour être autorisé.

Les gens font la queue pour se faire tester pour le COVID-19 devant l’hôpital St. Michael’s dans le centre-ville de Toronto. (Evan Mitsui/CBC)
Un gouvernement qui ne veut pas dicter quoi faire à ses scientifiques
S’adressant , mardi, aux journalistes par téléconférence sur les travaux de Santé Canada, la Dre Supriya Sharma, conseillère médicale principale du sous-ministre canadien de la Santé, a déclaré qu’elle ne pensait pas que le processus d’autorisation ait été lent jusqu’à présent.
Citant le risque d’approuver un test défectueux qui indiquerait aux gens qu’ils sont exempts de COVID-19 alors qu’ils sont effectivement infectés, elle a expliqué que le régime réglementaire du Canada est différent de celui en vigueur aux États-Unis. « Je ne pense pas que nous soyons lents. Nous avons du personnel qui travaille d’arrache-pied », dit-elle.
« Nous avons augmenté l’efficacité et nous rationalisons ces processus d’examen. Nous nous sommes engagés à ce qu’une entreprise obtienne une décision dans les 40 jours », a-t-elle ajouté en précisant que le processus prépandémique prenait souvent des mois.
Lorsqu’on lui a demandé si le ministère était réticent à approuver de nouveaux dispositifs en raison des erreurs passées, Mme Sharma a concédé que la décision rapide le printemps dernier de Santé Canada d’autoriser l’utilisation du test de Spartan Bioscience, basé à Ottawa – un test qui s’est avéré défectueux par la suite – a permis de tirer quelques « leçons » pour les autorités de réglementation. En mai, le laboratoire national de microbiologie a découvert des problèmes avec le test qui le rendaient très peu fiable.
Pressions de l’opposition
Mardi toujours, la députée conservatrice fédérale Michelle Rempel Garner, porte-parole du Parti conservateur en matière de santé, affirmait que le gouvernement libéral a trop attendu pour se procurer des tests rapides.
« Le même test rapide au point de service que Santé Canada étudie actuellement est utilisé par nos alliés du G7 depuis des mois. Et pourtant, il n’est toujours pas approuvé au Canada. Pourquoi notre pays a-t-il mis tant de temps à le faire ? Combien d’écoles ont dû fermer parce que nous n’avions pas cette capacité ? Combien d’heures ont été perdues parce que des parents qui travaillent ont dû faire la queue pour un examen ? » a demandé Rempel Garner.

Michelle Rempel Garner (CP)
Réagissant à cette critique, le premier ministre Justin Trudeau a défendu les organismes de réglementation, mardi.
« Les experts médicaux prendront les décisions qui conviennent le mieux aux Canadiens », a dit M. Trudeau aux journalistes, après avoir co- organisé une conférence des Nations Unies visant à collecter des fonds pour aider les pays en développement à lutter contre le virus.
« Sur le plan politique, bien que nous aimerions voir ces tests le plus rapidement possible, nous n’allons pas dire à nos scientifiques comment faire leur travail. Nous veillons cependant à ce que dès que ces approbations seront obtenues, nous soyons prêts à effectuer ces tests dans tout le pays », a-t-il déclaré.

Selon M. Trudeau, les scientifiques décideront quand les tests rapides COVID seront approuvés pour être utilisés au Canada. (CP)
Deuxième annonce majeure en deux semaines
Le 23 septembre dernier, Santé Canada avait approuvé l’utilisation au Canada du test Hyris bCube, un appareil portable qui, selon son distributeur de Guelph, en Ontario, peut être utilisé « partout où les gens se trouvent – à tout moment, n’importe où ».
Bien que Santé Canada ait approuvé ce test la semaine dernière qui ne nécessite pas de laboratoire, le dispositif a encore besoin d’environ 90 minutes pour obtenir un résultat.
LISEZ LA SUITE : Feu vert à un test capable de révéler la présence de la COVID-19 en 90 minutes
RCI avec CBC News et La Presse canadienne
EN COMPLÉMENT
COVID-19 : le test de 15 minutes existe aux États-Unis. Qu’attend le Canada?
Première au pays : tests de dépistage de la COVID-19 administrés en pharmacie
COVID-19 : pressions sur Santé Canada pour un feu vert urgent aux tests rapides









Pour des raisons indépendantes de notre volonté et, pour une période indéterminée, l'espace des commentaires est fermé. Cependant, nos réseaux sociaux restent ouverts à vos contributions.